Абстракт
Гиалуроновая кислота [ГК] найдена во внеклеточном матриксе позвоночных тканей, в поверхностном покрытии определенных видов Streptococcus и болезнетворных бактериальных микроорганизмов Pasteurella, а также на поверхности некоторых частично пораженных вирусом морских водорослей. Синтазы гиалуроновой кислоты [ГКС], это ферменты, которые полимеризуют ГК, используя UDP-сахарные предшественники, которые найдены во внешних мембранах этих организмов. Были идентифицированы гены ГКС из всех вышеупомянутых источников. Кажется, существуют два отличных класса ГКС, что основано на различиях в аминокислотной последовательности, предсказанной топологии в мембране и предполагаемом механизме реакции.
Все ГКС были определены как синтазы класса I, за исключением ГКС у вида Pasteurella. Был также объяснен каталитический способ работы единственной ГКС класса II (пмГКС). Этот фермент удлиняет внешние ГК-присоединяемые олигосахаридные акцепторы путем добавления индивидуальных моносахаридных единиц к неуменьшающемуся концу, чтобы сформировать длинные полимеры in vitro; ни одна ГКС класса I не имеет такой способности. Способ и направление полимеризации ГК, катализируемой ГКС класса I, остаются неясными. Фермент пмГКС также был проанализирован на предмет двух имеющихся у него активностей: GlcUA-трансферазной и GlcNAc-трансферазной. Таким образом, два активных участка существуют в одном пмГКС полипептиде, опровергая широко принятую догму гликобиологи: "один фермент - один модифицированный сахар". Предварительные свидетельства позволяют предполагать, что у ферментов класса I может также быть два участка активности.
Каталитический потенциал фермента пмГКС может использоваться, чтобы создать новые полисахариды или проектировать олигосахариды. Из-за множества потенциальных ГК-базирующихся медицинских методов лечения, эта хемоэнзиматическая технология обещает принести пользу на пути нашего стремления к хорошему здоровью.
Ключевые слова
Гиалуроновая кислота (ГК), хондроитин, гликозилтрансфераза, синтаза, катализ, механизм, химерные полисахариды, монодисперсные олигосахариды
Введение
Гиалуронан [ГК] - очень богатый глюкозаминогликан в организме позвоночных, имеющий и структурную, и сигнальную роли. Определенные патогенные бактерии, а именно, группы А и С вида Streptococcus и тип А Pasteurella multocida, производят внеклеточный покрывающий ГК, называемый капсулой. У обоих видов ГК капсула и является фактором ядовитости, который обеспечивает бактериям сопротивляемость фагоцитам и комплементарность. Другой организм, производящий ГК - это морская водоросля хлорелла, инфицированная определенным большим двухцепочечным ДНКовым вирусом PBCV-1. Роль ГК в жизненном цикле этого вируса пока не ясна на данный момент.
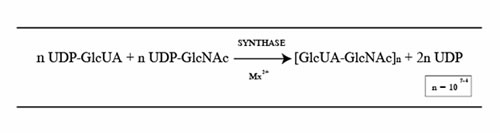
Иллюстрация 1. Реакция биосинтеза ГК.
Ферменты класса гликозилтрансфераз, которые полимеризируют ГК, называются ГК-синтазами (или ГКС), по старой терминологии, включающей также ГК-синтетазы. Все известные ГК-синтазы - это разновидности одного полипептида, ответственные за полимеризацию цепи ГК. UDP-сахарные предшественники, UDP-GlcNAc [UDP-N-ацетилглюкозамин] и UDP-GlcUA [UDP-глюкуроновая кислота] используются ГК-синтазами в присутствии двухвалентного катиона (Mn и/или Mg) при нейтральном pH (рис. 1). Все синтазы являются мембранносвязанными белками в живой клетке и обнаружены в мембранной фракции после лизиса клеток.
Между 1993 - 1998 были идентифицированы и клонированы на молекулярном уровне ГК-синтазы групп A и С Streptococcus [спГКС и сеГКС соответственно], ГК-синтазы позвоночных животных [ГКС 1,2,3], ГК-синтаза водорослевого вируса [свГКС], а также ГК-синтаза типа A вида Pasteurella multocida [пмГКС]. Первые три типа ГК-синтаз, кажется, очень похожи в размере, аминокислотной последовательности и предсказанной топологии в мембране. ГК-синтаза вида Pasteurella, напротив, больше и обладает существенно отличающейся от других синтаз последовательностью и предсказанной топологией. Поэтому, мы предположили существование двух классов ГК-синтаз (таблица 1). Ферменты класса I включают стрептококковые, позвоночные и вирусные белки, в то время как белок вида Pasteurella в настоящее время единственный член класса II. У нас также есть некоторые свидетельства того, что каталитические процессы ферментов класса I и класса II отличаются.
Таблица 1. Два класса ГК-синтаз:
| Класс I | Класс II | |
| Участники | спГКС, сеГКС, свГКС, ГКС позвоночных 1,2,3 |
пмГКС |
| Размер полипептида | 417-588 остатков | 972 остатка |
| Предсказанная топология | Многократные трансмембранные вкрапления или связанные с мембраной области | В растворе с C-терминальным участком приложения к мембранному компоненту |
| Молекулярное направление роста полимера | Неясно | Непрекращающееся терминальное удлиннение |
| Утилизация акцептора | Нехарактерно | Да |
Хотя ГК-синтаза вида Pasteurella был последним обнаруженным ферментом из всех, некоторые особенности пмГКС способствовали существенному продвижению в его изучении в сравнении с некоторыми членами ферментов класса I, которые исследовались четыре десятилетия. Ключевая особенностью пмГКС, которая позволила разъяснить молекулярное направление полимеризации и идентификацию ее двух активных участков - это способность пмГКС удлиннять внешне расположенный акцепторный олигосахарид. Рекомбинантная пмГКС добавляет одиночные моносахариды повторным способом к ГК-ассоциированному олигосахариду in vitro. Внутренняя особенность каждой передачи моносахарида ответственна для того, чтобы формировать альтернативное повторение дисахаридов в этом глюкозаминогликане; одновременное формирование дисахаридной единицы не требуется. С другой стороны, никакое подобное удлиннение внешних акцепторов не было доказано ни для какого фермента класса I. Через фундаментальное научное исследование мы теперь развили некоторые биотехнологические применения замечательного белка класса ГК-синтаз вида Pasteurella.
Материалы & методы
Реагенты
Все реактивы для молекулярнобиологических исследований без специальной пометки были от Promega. Стандартные олигонуклеотиды были от Great American Gene Company. Все другие реактивы высокой чистоты, если иначе не отмечено, были от Sigma или от Fisher.
Усечение пмГКС и точечные мутанты
Был произведен ряд усеченных полипептидов, путем амплификации pPm7А вставки методом полимеразной цепной реакцией с Taq-полимеразой (Fisher) и синтетическими олигонуклеотидными праймерами, соответствующими различным частям пмГКС, с открытой рамкой считывания. Ампликоны затем были клонированы в плазмиду для экспрессии pKK223-3 (tac промотор, Pharmacia). Получившимися рекомбинантными конструкциями были трансформированы клетки Escherichia coli штамма TOP 10F' (Invitrogen) и выращены на среде LB (Luria-Bertani) с ампициллиновой селекцией. Мутации были сделаны, используя метод QuickChange сайт-направленного мутагенеза (Stratagene) с плазмидой pKK/пмГКС как ДНК шаблон.
Приготовление фермента
Для приготовления мембраны, содержащей рекомбинантный пмГКС полной длины, пмГК1-972 был изолирован из E.coli, как описано. Для растворимых усеченных пмГКС белков, пмГКС1-703, пмГКС1-650 и пмГКС1-703 - содержащих мутантов, клетки были извлечены с помощью В-PerТМ II Bacterial Protein Extraction Reagent (Pieree) согласно инструкции производителя, за исключением того, что процедура была выполнена при 7°C в присутствии ингибиторов протеаз.
Ферментные пути полимеризации ГК. GlcNAc модификация или GlcUA модификация
Три варианта было разработано, чтобы обнаружить происходит ли (а) полимеризация длинных цепей ГК или (b) добавление одиночного GlcNAc к GlcUA-конечному акцепторному олигосахариду ГК [GlcNAc-Tase], или (c) добавление одиночного GlcUA к GlcNAc-конечному акцепторному олигосахариду ГК [GlcUA-Tase]. Полная активность ГКС была оценена для раствора, содержащего 50 mM Tris, pH 7.2, 20 mM MnCl2, 0.1 M (NH4)2SO4, 1 M этиленгликоля, 0.12 mM UDP-(14C)GlcUA (0.01 ?Ci; NEN), 0.3 mM UDP-GlcNAc и различный набор ГК олигосахаридов, полученный из тестикул путем обработки гиалуронидазой [(GlcNAc-GlcUA)n, n= 4-10] при 30°C в течение 25 минут в объеме реакционной смеси 50 мкл. GlcNAc-трансферазная активность была оценена в течение 4 минут в той же буферной системе с различным набором ГК олигосахаридов, но только с одним сахаром в роли предшественника - 0.3 mM UDP-(3H)GlcUA (0.2 ?Ci; NEN). GlcUA-трансферазная активность была оценена в течение 4 минут в той же самой буферной системе, но только с 0.12 mM UDP-(14C)GlcUA (0.02 ?Ci) и с нечетным набором ГК олигосахаридов [GlcNAc(GlcUA-GlcNAc)n, n= 7-20] (3.5 мкг уроновой кислоты), приготовленных при помощи воздействия ацетата ртути на ГК-лиазу Streptomyces. Реакции были прекращены путем добавления SDS до 2% (w/v). Продукты реакции были отделены от субстратов путем бумажной (Whatman 3M) хроматографии с этанолом/1 М сульфат аммония, pH 5 5, как основной растворитель (65:35 для ГКС и оценки GlcUA-Tase; 75:25 для оценки GlcNAc-Tase). Для оценки ГКС образец бумажной полосы был промыт водой, и объединение радиоактивных сахаров в полимер ГК было обнаружено по сцинтилляции жидкости, рассчитанной при помощи BioSafe II коктейля (RPI). Для реакций полуиспытания образец и расположенные вниз по течению 6 см полосы были посчитаны по частям в 2 см. Все оценочные эксперименты были просчитаны таким образом, чтобы быть линейными относительно времени инкубации и концентрации белка.
Гель-фильтрационная хроматография
Размер ГК полимеров был проанализирован хроматографически на колонках Phenomenex PolySep-GFC-P 3000, элюция производилась 0.2 M нитратом натрия. Колонка была стандартизована флуоресцентными декстранами различного размера. Радиоактивные компоненты были обнаружены с помощью датчика LB508 Radioflow (EG & G Berthold) и коктейля Zinsser. По сравнению с полной оценкой ГКС, используя бумажную хроматографию, описанную выше, эти 3-минутные реакции содержали дважды UDP-сахарные концентрации, 0.06 ?Ci UDP-(14C)GlcUA и 0.25 нанограмма ряда ГК олигосахаридов. Кроме того, использовалось добавление кипящего (2 минуты) этилендиамина тетрациловой кислоты ( финальная концентрация 22 mM ), чтобы закончить реакции вместо добавления SDS.
Результаты и обсуждение
Утилизация и специфичность акцептора ГКС
Некоторые олигосахариды были проверены, в качестве акцепторов для рекомбинантного пмГКС1-972 (Таблица 2). ГК олигосахариды были получены из тестикул путем гиалуронидазного щепления, а удлиннены пмГКС с помощью доставляемых подходящих UDP-сахаров. Восстановление борогидратом натрия не нарушает активность акцептора. С другой стороны, олигосахариды, полученные из ГК при помощи отщепления лиазой, не поддерживают удлиннение; дегидратированные ненасыщенные невосстановленные концевые остатки GlcUA нуждаются в гидроксильных группах, которые смогли бы присоединить входящий сахар из UDP-предшественника. Поэтому пмГКС-катализируемое удлиннение происходит в случае невосстановленных концевых групп. В ряде параллельных экспериментов было обнаружены рекомбинантные формы синтаз класса I - спГКС и х1ГКС, которые не удлинняют ГК-получаемые акцепторы. Принимая во внимание направление активности ферментов класса I, противоречивые сообщения были сделаны и необходимы дальнейшие исследования.
Таблица 2. Специфика олигосахаридных акцепторо пмГКС:
|
Сахар/Структуры
|
Активность удлиннения пмГКС |
|
ГК олигосахарид (гиалуронидаза-полученный)
[(?1,4)GIcUA(?1,3)GlcNAc]2,3
|
да
|
|
ГК олигосахарид (ГК-лиаза-полученный)
?GlcUA[(?1,3)GlcNAc(?1,4)GlcUA]1,2GlcNAc
|
нет
|
|
Уменьшенный ГК олигосахарид (гиалуронидаза, борогидрид)
GlcUA[(?1,3)GlcNAc(?1,4)GlcUA]1,2GlcNAc
|
да
|
|
Хитотетроза, хитопентоза [(?1,4)GlcNAc]4,5
|
нет
|
|
Хепарозан пентамер
GIcNAc[(?1,4)GlcUA(?1,4)GlcNAc]2
|
нет
|
|
Хондроитин сульфат пентамер
GalNAc-сульфат[(?1,4)GIcUA(?1,3)GlcNAc-сульфат]2
|
да
|
Интересно, что хондроитин сульфат пентамер является хорошим акцептором для пмГКС. Другие структурно связанные олигосахариды такие, как хитотетроза или хепарозан пентамер, однако, не служат акцепторами для пмГКС. В целом, пмГКС, кажется, требует, ?-связанных GlcUA-содержащих акцепторных олигосахаридов. Мы выдвигаем гипотезу, что участок связывания олигосахаридов промежуточен в цепи удерживания ГК во время полимеризации.
Молекулярный анализ активности пмГКС трансферазы: два активных участка в одном полипептиде
Возможность измерить два компонента гликозилтрансферазной активности ГК синтазы, GlcNAc-трансфераза и GlcUA-трансфераза, позволил молекулярный анализ пмГКС. Мы отметили, что короткий дублированный мотив последовательности: Asp-Gly-Ser [DGS] (Аспарагиновая к-та-Глицин-Серин), присутствовал в пмГКС. Из анализа сравнения гидрофобных групп многих других гликозилтрансфераз, которые производят ?-связанные полисахариды или олигосахариды предположили, что вообще, существует два типа доменов: области "A" и "Б". ПмГКС, синтаза класса II, тем и уникальна, что содержит два "А" домена (личная коммуникация, B.Henrissat). Было предложено, что определенные члены класса I ГК синтаз (спГКС) содержат одиночные "А" и одиночные "Б" области. Различное удаление или точечные мутанты пмГКС были оценены для их способности полимеризовать ГК цепи или их способность добавлять одиночный сахар к ГК акцепторному олигосахариду (Таблица 3). Суммируя сказанное, пмГКС содержит два отличных друг от друга активных участка. Мутагенез аспартата мотива DGS (остаток 196 или 477) по обоим сайтам приводи к потере ГК полимеризации, но активность другого сайта оставалась относительно незатронутой. Таким образом, двойная активность ГК синтазы была преобразована в два различных одиночных действия гликозилтрансферазы.
Таблица 3. Активность пмГКС с удаленным участком или точечной мутацией.
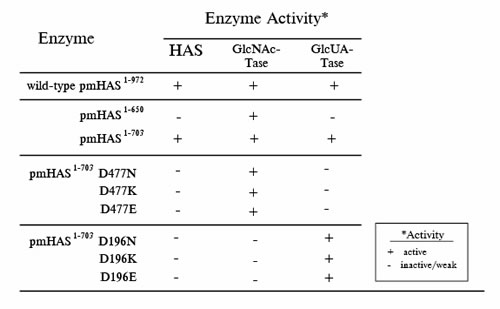
Удаление последних 269 остатков от конечной карбоксильной группы преобразовало слабо выраженный мембранный белок в хорошо выраженный растворимый. Рассмотрение аминокислотной последовательности белка пмГКС в этой области, однако, не показывает типичных особенностей вторичной структуры, которые обеспечили бы прямое взаимодействие фермента с двойным слоем липида. Мы выдвигаем гипотезу, что конечная карбоксильная группа каталитического фермента пмГКС стыкуется с направляющим мембраносвязанным полисахарида транспортного аппарата живущей бактериальной клетки.
Первая "A" область пмГКС, А1, является GlcNAc-тазой, в то время как вторая "A" область, A2, является GlcUA-тазой (рис. 2). Это - первая идентификация двух активных участков для фермента, который производит гетерополисахарид, так же как ясное доказательство, что один фермент может действительно передать два различных сахара. Отличный от типа F фермент вида P. multocida, названный пмЦС, был найден, и вяснено, что он катализирует формирование несульфатируемого полимера хондроитина. ГК и хондроитин идентичны в структуре, за исключением упомянутого выше полимера, который содержит N-ацетилглюкозамин вместо GlcNAc. И пмГКС, и пмЦС на 87 % идентичны на уровне аминокислот. Большинство изменений в остатках находятся в области А1, что вполне совместимо с гипотезой о том, что эта область ответственна за передачу гексозамина.

Иллюстрация 2. Схематическое изображение пмГКС областей.
Два независимых трансферазных домена, А1 и A2, ответственны за катализ полимеризации цепи ГК. Повторяющиеся последовательные добавления одиночных сахаров быстро строят цепь ГК. Похоже, что карбоксильный конец пмГКС некоторым способом взаимодействует с мембранносвязанным транспортным аппаратом бактериальной клетки.
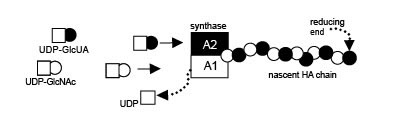
Иллюстрация 3. Модель биосинтеза ГК при помощи пмГКС.
Одиночные сахара добавляются к каждому "A" домену повторным способом к невосстанавливающемуся концу цепи ГК. Внутренняя точность каждой стадии активности трансферазы поддерживает повторение структуры дисахаридов ГК. Возникающая цепь ГК вероятно сохраняется пмГКС во время катализа через олигосахарид-связывающий участок.
Мы продемонстрировали эффективную передачу одиночного сахара с помощью пмГКС in vitro несколькими типами экспериментов, поэтому, мы выдвинули гипотезу, что цепи ГК формируются быстрым, повторяющимся добавлением одиночного сахара синтазой класса II (рис. 3). К настоящему времени, одна линия свидетельства предполагает, что фермент класса I также обладает двумя участками трансферазы. Мутация лейцинового остатка 314 на валин в ммГКС1, в части предварительного участка GlcUA-тазы, как сообщали, преобразовала эту ГКС позвоночного животного в хито-олигосахаридную синтазу. Ни один участок с соответствующей активностью GlcNAc-трансферазы не был идентифицирован.
Прививание полимера полисахаридными синтазами: добавление ГК к молекулам или твердым частицам
Исследование пмГКС в научно-исследовательской лаборатории преобразовало представления о ГК синтазах от царства трудных, упорных животноподобных чудовищ до потенциальных биотехнологических рабочих лошадок. Новые молекулы могут быть сформированы, используя способность пмГКС привить длинные цепи ГК на коротких ГК полученных цепях или хондроитин-производных акцепторах. Например, полезные акцепторы могут состоять из маленьких молекул или лекарств с ковалентно связанной ГК или хондроитин-олигосахаридные цепи (длиной в 4 сахара, например). В другом случае, цепи ГК могут быть добавлены к олигосахаридному праймеру, иммобилизованному на твердой поверхности (таблица 4). Таким образом, длинные цепи ГК могут быть мягко добавлены к чувствительным веществам или тонким устройствам.
В другом приложении, новые химерные полисахариды могут быть сформированы потому, что использование пмГКС олигосахаридным акцептором не столь же строго, как сахаридная трансферазная специфика. Хондроитин и хондроитин-сульфат признаны как акцепторы пмГКС и удлинняются ГК цепью различных длин (рис. 4). Наоборот, пмЦС очень гомлогичная хондроитин синтазе, распознает и удлинняет ГК акцепторы цепями хондроитина. Химерные молекулы глюкозаминогликана сформированы, содержа естественные, определенного соединения связи. Эти привитые полисахариды могут служить, чтобы присоединиться к клетке или ткани, которая связывает ГК с другой клеткой или ткань, связывающей хондроитин или хондроитин-сульфат. В определенных аспектах, привитые глюкозаминогликаны напоминают протеогликаны, которые являются существенными компонентами матрикса в тканях позвоночных. Но так как никакие компоновщики белка не присутствуют в химерных полимерах, то антигенность и проблемы протеолизиса, возникающие вокруг медицинского использования протеогликанов, устранены. Риск передачи инфекционных агентов тканями, извлеченными из животных, человеческому пациенту также уменьшен при использовании химерных полимеров.
Таблица 4. ПмГКС-инициированное прививание ГК на бусинки полиакриламида. Реакционная смесь содержит пмГКС, несущий радиоактивную метку UDP-(14C)GlcUA и UDP-(3H)GlcNAc, а также различные иммобилизованные праймеры сахаров (акцепторы, соединенные восстановительным аминированием в аминобусины) были представлены. Бусинки были промыты и радиоактивно инкорпорированы на другие бусины, измеренные методом расчета жидкостной сцинтилляции. ГК цепи были привиты на пластиковые бусины при использовании подходящего праймера и пмГКС.
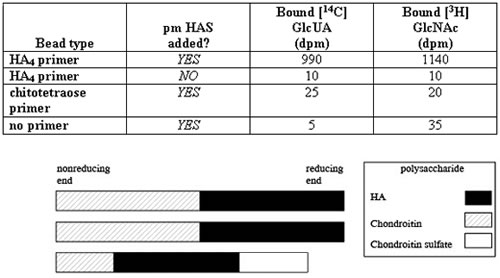
Иллюстрация 4. Схематическое изображение привитых полисахаридных структур. ГК синтаза вида Pasteurella или хондроитин синтаза будут удлиннять определенные другие полимеры на невосстанавливающемся конце in vitro, чтобы сформировать новые химерные глюкозаминогликаны. Изображены некоторые примеры.
Синтез монодисперсной ГК и ГК-связанных олигосахаридов
В дополнение к добавлению большой полимерной ГК цепи к молекулам акцептора, пмГКС синтезируют определенные меньшие ГК олигосахариды в диапазоне от 5 до 24 сахаров. Используя фермент дикого типа и различные условия реакции, был относительно легко получен ГК олигосахарид, содержащий 4 или 5 моноахаридов, удлиненных несколькими сахарами до более длинных версий, которые очень часто трудно получить в больших количествах. Мы выяснили, что, комбинируя растворимый мутант GlcUA-Tase и растворимый мутант GlcNAc-Tase в той же самой смеси реакции позволяет формирование ГК полимера, если система снабжена акцептором. В течение 3-х минут была сделана цепь из примерно 150 сахаров (-30 кДа). Любая одиночная мутант-синтаза не сформирует в результате цепь ГК. Поэтому, если дальнейший контроль реакции сделан путем выборочного комбинирования различных ферментов, UDP-сахаров и акцепторов, то могут быть получены определенные монодисперсные олигосахариды (рис. 5).
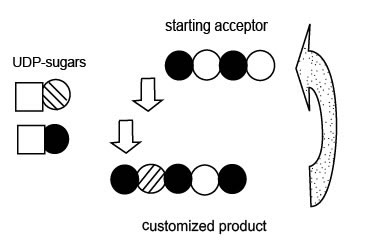
Иллюстрация 5. Приготовление определенных олигосахаридов.
В этом примере, акцептор ГК тетрасахарид удлинняется одиночной хондроитин дисахаридной единицей, используя два шага с иммобилизованным мутантом синтазы вида Pasteurella ( показано белыми стрелками ). Изображенный продукт является новым гексасахаридом. Повторение цикла еще раз производит олигосахарид, два цикла формируют декасахарид, и т.д. Если акцептор был ранее соединен с другой молекулой
( например препарат или лекарство ), тогда новый конъюгат был бы удлиннен коротким ГК, хондроитином или гибридной цепью как и желательно.
Например, в одном воплощении, смесь UDP-GlcNAc, UDP-GlcUA и акцептора постоянно циркулирует через отдельные биореакторы с иммобилизованными мутант-синтазами, которые передают только одиночный сахар. С каждым циклом инкубации биореактора другая сахарная группа добавляется к акцептору, чтобы сформировать маленькие определенные ГК олигосахариды. Использование похожего пмЦС мутанта (например GalNAc-Tase) в одном из шагов позволило происходить формированию смешанных олигосахаридов при использовании UDP-GlcNAc. Биологическая активность и терапевтический потенциал маленьких ГК олигосахаридов - сложная область для исследования, которая потребует определенных, монодисперсных сахаров для однозначной интерпретации.
Заключение
Очевидно, существуют два различных класса ГК синтаз. Наиболее хорошо охарактеризован фермент класса II вида Рasteurella, удлинняющий цепь ГК повторяющимся присоединением одиночного сахара на невосстанавливающийся конец цепи ГК. Направление и способ работы синтаз класса I (стрептококковые, вирусные и ферменты позвоночных) остаются неясными. Относительно прикладных наук, способность пмГКС удлиннять экзогенно расположенные акцепторные молекулы полезна для создания новых молекул и/или устройств с потенциальным медицинским применением.
Благодарности
Я благодарю Национальный Институт Здоровья (грант GM56497), и Национальный Фонд Науки (грант MCB-9876193) за поддержку этого исследования, а также Вей Джинг, Эми Пэджет-МакКью и Аннетт Флешман за их усилия в лаборатории.