Абстракт
Были исследованы эффекты ионов различных металлов на реологические профили потока растворов гиалуроната решения путем управляемой инкубации растворов солей хлоридов металлов с раствором гиалуроната натрия (ГН) при окружающих условиях. Результаты применения модели Уильямсона к профилям потока инкубируемых растворов показали прогрессивное уменьшение вязкости Уильямсона (?0) при сдвиге нуля с увеличением атомного числа/атомной массы иона металла, который, за исключением данных для лития, мог быть связаны с уравнением силы (y = сx?). Такие сокращения вязкости не были результатом гидролиза (определено ГФХ (GPC) - гель-фильтрационной хроматографией), но могут произойти из-за диффундирующих ионов, разрушающих водородные связи и предотвращающих электростатические отталкивания между карбоксильными группами.
Введение
Гиалуронан - биосинтезируемый/биоразлагаемый, линейный, растворимый в воде, ионный полимер составленный из повторения (l?4) связанных дисахаридных единиц, состоящий из ?-D-GlqpA и ? -D-GIcpNAc, соединенных вместе (l?3) гликозидными связями. У него высокий молекулярный вес (приблизительно 105-107 Да), в зависимости от источника, давая диапазон разности примерно 250-25000. Он обнаружен у всех позвоночных животных, присутствует в почти каждой ткани как компонент внеклеточного матрикса и распределен всюду в теле млекопитающих, особенно в синовиальной жидкости, свободной соединительной ткани, пуповине и стекловидном теле глаза. Наибольшее количество гиалуронана (7-8 г в среднем на человека, 50 % общего количества гиалуронана в организме), находится в тканях кожи (и дермис, и эпидерма). Наиболее изолируемая/используемая (in vitro) форма гиалуронана - свободная кислота (гиалуроновая кислота, ГК) и ее натриевая соль (гиалуронат натрий, ГН).
В растворах основа гиалуронана укреплена химической структурой связанных дисахаридных единиц, внутренних водородных связей, взаимно отталкивающихся анионных групп и взаимодействием молекул растворителя, делая её твердой и высоко гидратированной молекулой. В физиологических растворах он принимает структуру расширенной случайной катушки, занимая большую область. Маленькие молекулы, например, вода и электролиты, могут свободно распространиться через занимаемую гиалуронаном область, в то время как большие молекулы в ней частично исключены из-за их гидродинамического размера. При низкой концентрации полимера индивидуальные цепи запутывают формирование непрерывной сети, обеспечивая вязкоупругие и псевдопластичные свойства, которые уникальны для растворимого в воде полимера при низкой концентрации. При более высоких концентраций может быть сформирована сложная запутанная сеть, которая может сопротивляться быстрому, короткому по продолжительности потоку жидкости, таким образом показывая свои упругие свойства. Однако, короткий поток жидкости более длинной продолжительности может частично отделить и выровнять молекулы, разрешая движение, что таким образом характеризует вязкие свойства.
Вязкоупругие свойства растворов ГК идеальны для использования в качестве биологического амортизатора и смазки, именно поэтому ГК присутствует в синовиальной жидкости, где она смазывает хрящ между суставами. Хрящ обеспечивает подушку между костями, позволяющую суставу перемещаться гладко. Однако, в подагрическом суставе эластичность/вязкость суставной жидкости уменьшается, уменьшая поглощение трения и барьерные свойства. Очень вязкоупругие растворы ГК могут быть введены в суставы (вискосупплементация), чтобы восстановить реологическую окружающую среду сустава и таким образом улучшите суставную функцию. Это используется в суставах остеоартритиков, чтобы обеспечить момент защита и поглощение шока, таким образом уменьшая боль связанную с подвижностью.
Цель этого исследования состояла в том, чтобы видеть взаимодействие ГК с рядом металлических ионов (отличающегося ионного размера, валентности, и т.д.) затрагивал реологический поток характеристик (особенно сдвиг нуля вязкости, ?0), и профиль молекулярной массы. Это особенно интересно относительно локализованного in vivo применения ГК, с тех пор как обнаружены многочисленные ионы металлов в организме, с которыми могла бы взаимодействовать управляемая ГК, потенциально приводящая к существенным изменениям в желательных физических свойствах.
Материалы & Методы
Подготовка деионизированной воды кипящим жидким азотом
Деионизированная вода была кипящей (~ 5 минут, под вакуумом), чтобы удалить растворенный воздух, охлаждена до окружающей температуры, а затем инкубирована с азотом (~ 15 минут), чтобы переместить любой остаточный воздух и предотвратить растворение новых молекул воздуха. Как результат азот закипел, деионизированная вода была охлаждена (4?C) до тех пор пока не потребуется, а впоследствии использовалась для подготовки всех последующих растворов (ГН и солевые растворы металлов, детали ниже). Кипящий азот использовался, чтобы исключить растворение кислорода из воды, чтобы попробовать и минимизировать любые окислительные эффекты деградации ГК.
Подготовка растворов гиалуроната натрия (ГН)
Гиалуронат натрия (ГН, 6 г, произведен бактериальной ферментацией брожения Streptococcus equi), был рассеян в кипящем азоте, деионизированной воде (600 мл) в конической колбе (1 л), а оставшееся пространство колбы залили азотом. Колба была закупорена, что позволило ГН медленно растворяться за период примерно 48 часов (при 4?C), с периодическим аккуратным перемешиванием/циркулированием, чтобы помочь растворению, приводящему к вязкому, гомогенному раствору ГН (1 %). Позаботились о том, чтобы исключить использование любого металлического оборудования при производстве раствора ГН (особенно вещей, содержащих железо/нержавеющую сталь), чтобы минимизировать потенциальные эффекты деградации.
Приготовление растворов ионов металлов
Металлические растворы солей хлоридов (0.25 M) были приготовлены растворением необходимого количества солей: безводного хлорида лития (LiCl, Mw 42.39), поваренная соль (NaCl, Mw 58.44), хлорида калия (KC1, Mw 74.55), безводного хлорида кальция (CaCl2, Mw 111.0), тетрагидрата хлорида марганца (II) (MnCl2.4H2O, Mw 197 9), гексагидрата хлорида кобальта (II) (CoCl2.6H2O, Mw 237.9), и гептагидрата хлорида церия (III) (CeCl3.7H2O, Mw 372.6) - в кипящем жидком азоте, деионизированной воде (50 мл) в объемных колбах (50 мл). Все растворы были фильтрованы (использовался фильтр с порами размера 0.45 мкм, нейлоновые мембранные фильтры 25-миллиметрового диаметра) и залиты азотом (чтобы удалить любой растворенный воздух/кислород), прежде, чем использоваться в эксперименте инкубации ГК.
Инкубация ГК с металлическими ионами
Определенные количества растворов ГН (1 %, 5 мл) были перенесены в свободные пузырьки (20 мл, Merck). Определенные количества металлических растворов хлорида детализированы выше (0.25 м., 5 мл) были перенесены в индивидуальные свободные пузырьки, содержащие раствор ГН (в двойном экземпляре), чтобы получить конечные концентрации 0.5 % ГН и ионов металлов на 0.125 М. Наконечник пипетки, используемый для индивидуального распределения растворов ГН, был также использован для последующего распределения раствора ионов металла, так, чтобы последний гарантировал, чтобы любой остаточный ГН был вымыт из наконечника пипетки. Двойной контроль был также подготовлен, используя кипящий жидкий азот, деионизировав аликвоту воды (5 мл). Конечные растворы промылись азотом (чтобы удалить любой растворенный воздух/кислород, который также облегчал смешивание), а пузырьки, запечатанные бутил/ПТФЭ (политетрафторэтилен), выровняли (3 мм) плоскими алюминиевыми ленточными крышками (20-миллиметровый диаметр, Merck). Растворы были инкубированы в окружающей температуре, и реологические профили потока определили точно спустя 1 час после добавления раствора иона металла (как детализировано ниже). [Эта испытательная процедура инкубации была ранее утверждена проведением серии повторных реологических исследований на испытательных растворах (ГН и солей металлов), которая привел к бесконечному значению сдвига вязкости Уильямсона ?0 с % изменением значений <10 %].
Определение реологических профилей потока
Все реологические измерения профиля потока были выполнены, используя TA Instruments AR 1000 'Rheolyst' с контролируемым напряжением реометра, оборудованного программным обеспечением 'Rheology Solutions'. Программное обеспечение разделено на два модуля, модуль 'AR1000' управляет инструментом непосредственно и позволяет оператору настроить экспериментальные процедуры и выполнить фактические эксперименты, в то время как модуль 'Данные' контролирует и предоставляет собранные данные. Были выполнены двойные реологические измерения профиля потока, используя ряд испытательных параметров, детализированных ниже. Приблизительно 5 мл образца использовались для каждого пробного потока (остаток был сохранен при 4?C до выполнения определения молекулярной массы). Модуль 'Данные' использовался, чтобы применить модель Уильямсона к проистекающим профилям потока (сдвиг нормы против вязкости), чтобы определить значение сдвига нуля вязкости Уильямсона ?0. Модель Уильямсона описывает поведение вязкости низкого сдвига, полученное из модели Кросса когда ? >> ??. Геометрия: параллельная пластина (диаметр на 4 см) Промежуток геометрии: 500 мкм Инерция геометрии: ~ 1.5 мкНмс2 (калиброванный перед каждым тестом) Инерция инструмента: ~ 14.2 мкНмс2 (калиброванный ежедневно) Температура: 20?C (управляется пластиной Пелтиера) Предэкспериментальный сдвиг напряжение: 1.768 Па (для 10 с) Испытательный диапазон напряжения: 0.5-500 Па (логарифмическая шкала) Число пунктов: 31 (максимальное время пункта 1 минута)
Определение профилей молекулярной массы
Профили молекулярного веса инкубируемых растворов (0.5 % ГН, 0.125 М соль металла, & контроли), детализированных выше были определены спустя примерно 12-24 часа после инкубации, анализом ГФХ, используя систему ВЭЖХ, детализированную ниже. Инструменты: Knauer ВЭЖХ насос 64 Водный автоинжектор Wisp 712 Колонки Knauer & блок управления (установлено для 30?C) Дифференциальный рефрактометр Knauer Универсальный интерфейс Dionex UI20 (для канала связи PC) Колонки GPC: ПрогельТМ TSK G5000, G4000 & G2500 PW (13 мкм, 300 x 7.5 мм ID) колонки (& предохранитель) связанные в серию. Элюент: Фосфатный буфер 0.05 М, содержащий 0.25 М NaCl, pH = 7.0 (приготовлен с использованием 18 М? UNQ установки для воды с пропусканием гелия) Расход: 0.5 мл/минуту Калибровка: Стандарты Pullulan со значениями MP 853, 380, 186, 100, 48, 23.7,12.2 & 5.8 кДа (0.1 мкг/мкл в воде UHQ) Объемы инъекции: 200 мкл (растворы разбавляли 1 к 10 водой UHQ) Сбор данных: Программное обеспечение Dionex Chromeleon Обработка данных: Программное обеспечение Caliber Reanalysis
Результаты & Обсуждения
Значимые профили потока (двойные исследования, сдвиг нуля против вязкости) для инкубируемых ГН/растворов ионов металлов (и контроля) показаны на иллюстрациях 1 и 2, где показано, что инкубация с металлическими ионами приводит к сокращению вязкости. Анализ GPC показал, что в образце контроля (ГН + вода, то есть нет никаких дополнительных добавленных ионы металлов) были значения Mp и полудисперсности (Mw/Мn) 2.5*106 Да и 1.6 соответственно. Инкубированные образцы имели значение Mp в области 1.9-2.5*106 Да и значение полудисперсности в области 1.7-2.0, то есть никакая существенная деградация не имела место быть. Модель Уильямсона была применена к профилям потока, чтобы определить сдвиг нуля вязкости Уильямсона ?0. Это - область, где увеличение напряжения сдвига/сдвига нормы имеет небольшой или не имеют никакого эффекта на вязкость (то есть, ведут себя согласно закону Ньютона для жидкого потока).
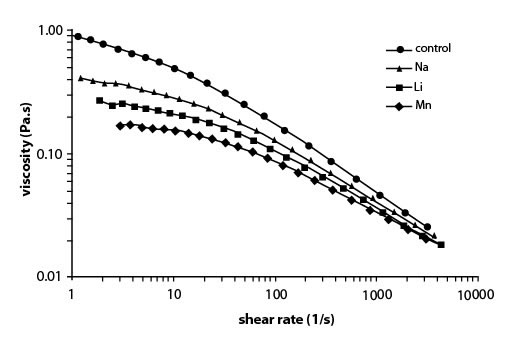
Иллюстрация 1. Значимые профили потока (сдвиг нуля против вязкости) для растворов ГН, инкубированных с водой (контроль), с ионами Na+, Li+ и Mn2+ (все - соли Cl-).
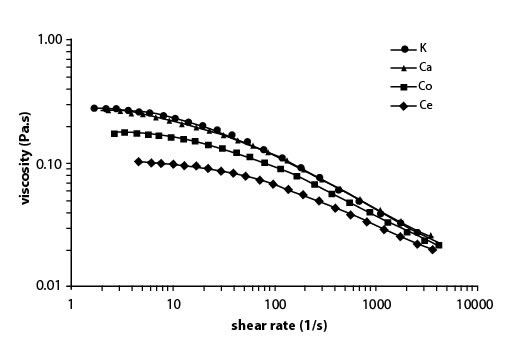
Иллюстрация 2. Значимые профили потока (сдвиг нуля против вязкости) для растворов ГН, инкубированных с ионами K+, Ca2+, Co2+ и Ce3+ (все - соли Cl-).
Сдвиги нуля вязкостей Уильямсона ?0, были связаны с атомным числом и атомной массой связанных металлических ионов, которые используется в инкубации (иллюстрация 3). Данные (за исключением лития), могли быть удовлетворительно смоделированы, используя уравнением силы y = сx? (иллюстрация 3). Никакой очевидной корреляции не было получено между сдвигом вязкости Уильямсона ?0 и ионными радиусами/ионным объемом ионов металлов, используемых в инкубации.
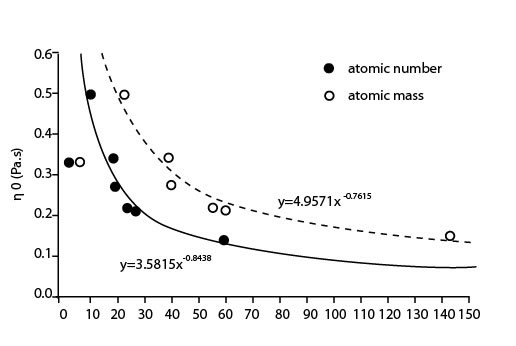
Иллюстрация 3. Отношения между сдвигом нуля вязкости Уильямсона ?0 и атомным числом/атомной массой металлического иона, используемого для инкубации.
Эти результаты согласуются с предыдущими изданными данными, сдвиг нуля вязкость (?0), как выяснили, уменьшается для ряда ионов, например, Na+, K+ и Ca2+, и Na+, Li+ и K+. Было предположено, чтобы эти наблюдаемые сокращения вязкости были результатом действия ионов, распространяющихся между цепями ГК и экранирования электростатические отталкивания (между соседним карбоксильными группами), а также разрушения водородных связей взаимодействий между цепями. Это может привести к краху расширенной укрепленной структуры катушки и переходу к более компактной структуре, где цепи могли бы скользить друг по другу более легко (то есть поток), таким образом приводя к сокращению вязкости.
Заключение
С увеличением атомного числа/атомной массы иона металла наблюдалось прогрессивное уменьшение в сдвиге нуля вязкости Уильямсона ?0. Таким образом, контакты с ионами металлов изменяют реологические особенности ГК, что может, в свою очередь, неблагоприятно затронуть его функциональные прикладные свойства. Организм содержит изобилие металлических ионов (особенно K+, Na+, Ca2+ и Mg2+), у которых поэтому есть потенциал, чтобы изменить вязкость управляемых материалов с ГК основой. Эффект Li+, кажется будет более значимым, чем ожидалось ( базируется исключительно на его заряде, размере, и т.д ), который особенно интересен с появлением значительного числа фармацевтических продуктов, содержащих литий. Эффекты более широкого диапазона ионов металлов более высокой валентности (например. Al3+, Ti4+ и Sn4+) должны быть исследованы, чтобы увидеть, могут ли дальнейшие корреляции быть сделаны. Эффекты ионов таких металлов на вязкоупругие свойств ГК материалов ( использование инерции & измерение колебаний ), также заслуживают исследования.