Функция гидрогелей по большей части зависит от их перекрестно-сшитой структуры. Уровень перекрестного сшивания определяется средней молекулярной массой полимерной цепи между сшивками. Плотность поперечных сшивок напрямую влияет на другие фундаментальные свойства гидрогелей, такие как степень набухания, механическая прочность и эластичность, проницаемость и даже диффузия (Lowman and Peppas, 1999; Peppas et al., 2000). Эти качества, которые могут быть высчитаны экспериментально или теоретически, способствуют пониманию структуры гидрогелей.
Определение
Гидрогели являются гидрофильными поперечно-сшитыми полимерами, которые способны набухать в воде и формировать нерастворимую объемную сеть. Нерастворимое строение и объемная структура являются результатом поперечных сшивок полимеров. Сеть остается в равновесии с водным окружением, при этом наблюдается баланс эластичных сил поперечно-сшитых полимеров с осмотическими силами раствора (рис.3.1). Химический состав и молекулярный вес определяют плотность поперечных сшивок, которая, в свою очередь, влияет на набухание и величину пор геля (Rosenblatt et al., 1994; Peppas et al., 2000). Кроме того, именно перекрестные сшивки определяют характеристики гидрогелей как твердого вещества, а не раствора, определяя эластичный ответ на натяжение (Gehrke et al., 1997).
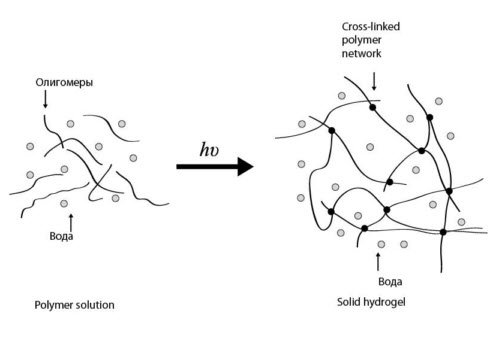
Рис.3.1. Схематическое изображение перехода жидкого геля в гидрогель путем фотополимеризации. Поперечно-сшитая сеть может быть создана путем физических сшивок, ковалентных или ионных связей (Varghese and Elisseeff, 2006). Water – вода, oligomers – олигомеры, polymer solution – раствор полимера, solid hydrogel - твердый гидрогель, cross-linked polymer network – поперечно-сшитая сеть полимеров.
Характеристика
Набухание
Физические характеристики гидрогелей помогают определить набухание гидрогелей или количество поглощенной ими воды. Набухание напрямую зависит от химической структуры полимера и обратно зависит от уровня плотности поперечных сшивок. Flory и Rehner (1943) в 1943 при определении количественных характеристик резины впервые связали плотность поперечных сшивок с набуханием полимера. В модели Flory-Rehner (1943) уровень набухания находится в равновесии между эластичными силами полимера и термодинамическими силами, образующимися при смешивании полимера и растворителя. В 1977 Peppas и Merrill (1977) модифицировали теорию Flory-Rehner в приложении к производству гидрогелей из растворов полимеров. Благодаря эластичным силам, наличие воды влияет на изменение химического потенциала внутри системы (Peppas and Mirrill, 1977; Peppas et al., 2000). Химическая структура влияет на набухание в результате наличия химических групп внутри гидрогелей. Например, гидрогели с гидрофильными группами набухают больше по сравнению с гидрогелями с гидрофобными группами; последние в присутствии воды не увеличиваются в объеме (Peppas et al., 2000). Для класса «умных» гидрогелей, чей объем изменяется в зависимости от окружающих условий, набухание может также зависеть от рН, температуры или облучения (Lowman and Peppas, 1999).
Предел набухания может быть определен экспериментально или подсчитан теоретически. Точное измерение предела набухания помогает в расчетах плотности поперечных сшивок, размеров ячеек и коэффициентов диффузии. Для измерения набухания гидрогелей используются следующие экспериментальные методы: гравиметрическое измерение после погружения в жидкость, использование специализированных приборов для измерения изменения объема и измерение коэффициента поглощения красителя декстрана (dextran dye), исключенного из твердой фазы (Noomrio et al., 2005). Значение набухания в равновесии является стандартной величиной, однако для некоторых стимул-зависимых форм, например контролируемого высвобождения лекарственных средств, используют динамические измерения (Traitel et al.,2003).
Эластичность
Разбухшие гидрогели при стрессе проявляют эластичные качества: эластическое напряжение и его противоположность – сжатие. Эластичность, как и набухание, зависимо и может быть подсчитано, если известна плотность поперечных сшивок. Высокая плотность поперечных сшивок приводит к более высокой механической прочности, но в то же время и к пониженным эластичности и набуханию. Значительное повышение количества поперечных сшивок в некоторых гидрогелях вызывает образование хрупких гелей (Peppas et al., 2000). Вследствие этого, оптимальная плотность поперечных сшивок обеспечивает баланс между эластичностью и желаемой прочностью (Peppas et al., 2000). При синтезе нового макромера гидрогелей, поли(6-аминогексил пропилен фосфата), Li et al. (2006) для достижения механической прочности и для уменьшения уровня набухания геля повысил в нем количество поперечных сшивок, увеличив содержание акрилата. Kim et al. (2004) похожим образом добился большей механической плотности увеличением поперечных сшивок фиброинов шелка, благодаря повышенной температуре гелеобразования и большей концентрации фиброина.
Проницаемость
Пористость гидрогелей или размер ячеек - структурное свойство гирогелей, определяющееся расстоянием между соседними поперечными сшивками. Пористость является следствием плотности поперечных сшивок, состава и концентрации мономеров (Lowman and Peppas, 1999). При изучении в 1998 поли(этилен гликоль) диакрилата (poly(ethylene glycol) diacrylate – PEGDA) Сruise et al. (1998) показал значительные изменения в пористости при изменении молекулярного веса полимера, а также небольшие изменения размеров ячеек при различных концентрациях PEGDA. В данной стабильной сети с одинаковыми изменениями в пористости размер ячеек растет с большим набуханием и уменьшается при пониженном набухании (Gehrke et al., 1997). Kim et al. (2004) показывает похожие взаимодействия в экспериментах с шелковыми гидрогелями, показывая уменьшение размера пор с увеличением сшивок фиброина. Прямые измерения пористости включают электронную микроскопию или квази-эластическое лазерное рассеивание (Stock and Ray, 1985). Напротив, непрямые методы, такие как ртутная порометрия, измерения каучуко-подобной эластичности и предельного набухания, могут дать дополнительные вычисления (Canal and Peppas, 1989; Mikos et al., 1993; Lowman and Peppas, 1997, 1999).
Диффузия
В клеточном конструировании тканей уровень диффузии растворенного вещества важен для определения высвобождения лекарственных веществ или транспорта питательных веществ и метаболитов. Диффузия питательных веществ, метаболитов и других растворенных веществ зависит от множества факторов, включая морфологию сети, состав полимеров, содержание воды, концентрацию растворенных веществ и полимеров, набухание и разрушение гелей (Lowman and Peppas,1999). Эти основополагающие факторы могут комбинироваться, вызывая химическое или физическое влияние, замедляющее диффузию растворенного вещества. Химический эффект описывает силы притяжения между растворенными веществами и матриксом гидрогеля, в то время как вытеснение физического объема показывает основной эффект трения на диффузию в гидрогеле (Gehrke et al., 1997),
Методы формирования гидрогелей
Образование поперечных сшивок в полимерах лежит в основе структуры гидрогелей. Оно влияет на формирование гидрогеля, его форму, размер и деградацию. Для удачного биомедицинского использования необходим контроль над образованием поперечных сшивок. Данный раздел описывает различные типы сшивок в гидрогелях: ковалентные, ионные и физические взаимодействия (Hennink and van Nostrum, 2002). Кроме того, здесь рассматриваются различные материалы для построения гидрогелей, которые показывают каждый тип сшивок, с акцентом на применении в тканевой инженерии. Наконец, будут рассмотрены сходные с биологическими гидрогели, эта область имеет большие перспективы для биомедицинской инженерии.
Ковалентные поперечные сшивки
Образование ковалентных поперечных сшивок может инициироваться радикальной полимеризацией, также образование сшивок может быть результатом дополнительных реакций, реакций конденсации, высокоэнергетического излучения (гамма-излучения и пучка электронов) и ферментного катализа (Hennink and van Nostrum, 2002). Перед началом радикальной полимеризации полимеры обычно нуждаются в модификации путем добавления дополнительных групп. Например, в полиэтиленгликоле (poly(ethylene glycol) – PEG) для обеспечения ковалентных сшивок вдоль полимера к функциональным группам добавляется акрилат (West and Hubbell, 1995). Радикальная полимеризация акрилатных групп может быть инициирована светом, температурными инициирующими системами и окислительно-восстановительным катализом (Nguyen and West, 2002; Shung et al., 2003). После того, как процесс образования сшивок запущен, его нельзя отменить или остановить (Elisseeff et al., 2005).
Фотополимеризация представляет собой преобразование жидкого раствора полимера в гель под воздействием фотосенсибилизирующих катализаторов и света (Hennink and van Nostrum, 2002). Фотополимеризация является идеальным методом для клинической имплантации, так как повышает пространственно-временной контроль (объемная сеть и быстрое включение/выключение, соответственно) (Williams et al., 2003). Гидрогели могут быть инъецированы, им придается форма и происходит их затвердевание in situ (Elisseeff et al., 2000). Данный подход связан с минимальными инвазивными воздействиями, и может применяться в черепно-лицевой медицине с трансдермальной фотополимеризацией или артроскопических процедурах с использованием оптоволоконного источника света (Anseth et al., 2002; Williams et al., 2003).
Два ковалентно сшитых гидрогеля, использовавшихся в тканевой инженерии, - PEG и гиалуроновая кислота (hyaluronic acid – HA), глюкозаминогликан, найденный в ECM. Модифицирование гелей биоактивными молекулами и/или химическими группами для сшивок повышает их биохимическую функциональность и механическую стабильность, замедляет деградацию, что увеличивает роль гидрогелей в качестве подложки (Segura et al., 2005). Молекулы полиэтиленгликоль акрилата (PEGA) подвергаются радикальной полимеризации и формируют химический поперечно-сшитый гидрогель (Sawhney et al, 1993; Martens et al., 2003). Гиалуроновой кислоте для начала радикальной реакции образования сшивок необходима модификация ее функциональных боковых групп (Baier Leach et al., 2002). Baier Leach et al для создания гидрогелей проводил реакцию между метакрилатными группами и гиалуроновой кислотой. Shu et al. (2004b) синтезировал тиолаты гиалуроновой кислоты и затем конъюгировал их с PEG для in situ инъекции, инкапсуляции клеток и пролиферации. PEG и НА могут быть в дальнейшем изменены для специализированных целей тканевой инженерии. Hern and Hubbell (1998) впервые модифицировали PEGA адгезивным пептидом аргинил-глицил-аспартановой кислотой (arginyl-glycyl-aspartic acid – RGD) для повышения адгезии клеток и стимуляции роста тканей. В отдельных экспериментах, PEG метакрилат был изменен с помощью фосфоэфиров и RGD для улучшения костной инженерии (Burdick and Anseth, 2002; Wang et al., 2005). В добавок ко всему, НА была сополимеризована с PEGDA + RGD для поддержания прикрепления клеток и пролиферации, а также для усиления восстановления хряща (Park et al., 2003; Shu et al., 2004a).
Ионные поперечные сшивки
Вторым типом сшивок в гидрогелях являются ионные взаимодействия. Альгинат, природный полисахарид из водорослей, формирует гидрогель с помощью ионных связей в присутствии бивалентных или мультивалентных катионов (Lee et al., 2000b). В реакции, происходящей при комнатной температуре и физиологичном рН, ионы кальция взаимодействуют с альгинатом и формируют ионные мостики между цепочками полимеров (Drury et al., 2004). Ионные взаимодействия слабее ковалентных сшивок, поэтому альгинатные гели переживают быстрый распад сшивок в физиологическом растворе - среде, в которой и предполагается действие биомедицинских гидрогелей. LeRoux et al. (1999) показал более чем 60% снижение механической прочности после 15-минутного пребывания геля в растворе хлорида натрия. Причиной распада сшивок служат бивалентные ионы, обменивающиеся на одновалентные катионы натрия (Lee et al., 2000b). Одним из примеров синтетического полимера, формирующего гидрогель с ионными взаимодействиями с катионами, является поли[ди(карбоксилатофенокси)фосфазен] (Andrianov et al., 1994).
Физические перекрестные сшивки
Некоторые сшивающие агенты неблагоприятно влияют на клетки или белки, инкапсулированные в гелях, и должны быть извлечены из геля перед его применением (Hennink and van Nostrum, 2002). Для избежания потенциально токсичных метаболитов ученые исследовали физически сшитые гидрогели. В основе физических сшивок лежат водородные связи, гидрофобные взаимодействия и Ван-дер-ваальсовые силы. Ионные сшивки, относимые некоторыми исследователями к физическим взаимодействиям, были рассмотрены в предыдущей части. В то время как каждая отдельная физическая связь очень мала, комбинация этих взаимодействий образует сильную связь (Zhang, 2002). Zhang (2002) описал молекулярную самосборку как совокупность молекулярных строительных блоков, претерпевающих серию шагов к самопроизвольному формированию стабильной и определенной сети. Распад сшивок предотвращается физическим взаимодействием между цепочками полимеров (Hennink and van Nostrum, 2002). В то время как большинство исследований Zhang посвящено белкам, основы самособирающихся пептидов могут быть применимы к синтетическим полимерам и природным молекулам. Это будет описываться более подробно в последней главе этой части. Pluronics® является другим примером физического взаимодействия, где амфифильные сополимеры, поли(этилен оксид) (poly(ethylene oxide) – PEO) и поли(пропилен оксид) (poly(propylene oxide)), сшиваются с помощью гидрофобных взаимодействий в водном растворе в ответ на температуру (Kabanov et al., 2002).
Одним из методов, используемых для создания биоподобных гидрогелей, является получение физических сшивок биоактивных факторов. Факторы роста остаются активными после инкапсуляции, повышая пролиферацию и дифференцировку инкапсулированных клеток или усиливая локальную регенерацию тканей (Lee et al., 2000a; Burdick et al., 2002b). Заключенные в гидрогели факторы роста содержат костный морфогенетический белок-2 (bone morphogenetic protein-2) – BMP-2, фактор роста фибробластов, сосудисто-эндотелиальный фактор роста (vascular endothelial growth factor) – VEGF, инсулино-подобный фактор роста-1 (insulin-like growth factor-1) - IGF-1 и трансформирующий фактор роста-3 (transforming growth factor-3) - TGF-3, и другие (Peters et al., 1998; Yamamoto et al., 1998; Tabata et al., 1999; Elisseeff et al., 2001; Lutolf et al., 2003). Следующий параграф посвящен иллюстрации эффектов биоподобных гидрогелей на три вида различных тканей.
Lee et al. (2000a) изучал неоангиогенез в альгинатных гидрогелях с включением VEGF, имплантированных в мышей с тяжелым комбинированным иммунодефицитом и нетучным диабетом. Результаты гистологического анализа показали повышенное сосудообразование при использовании гидрогелей с VEGF по сравнению с гидрогелями без VEGF. При увеличении концентрации выхода VEGF из гидрогеля наблюдалось статистически значимое повышение сосудообразования. Для улучшения формирования хряща Elisseff et al. (2001) заключил в гидрогели IGF-1 и трансформирующий фактор роста пи (TGF-pi) в полиэтиленоксид диметилакрилатные гидрогели с телячьими хондроцитами. Гидрогели, содержащие IGF-1 и TGF-pi показали значительное повышение продукции глюкозаминогликанов про сравнению с гидрогелями с одним фактором роста или гидрогелями без факторов роста. В своих инновационных исследованиях по улучшению заживления костей черепа у крыс Lutolf et al. (2003) сшивал субстраты для металлопротеазы матрикса (matrix metalloprotease – MMP) и RGD с гидрогелями на основе PEG вместе с BMP-2. ММР субстраты управляются ММР-зависимой деградацией межклеточного матрикса, что позволяет инвазию клеток и реконструирование матрикса. Выход BMP-2 значительно повышает заживление кости. Эти результаты показывают, что стимулирование деградации матрикса и локальной клеточной адгезии в сочетании с выходом ростовых факторов значительно повышает локальный рост кости, подтвержденный гистологическими и радиологическими анализами.